【目次】
1. 背景:ナノ医薬品の産業化を阻む「製造プロセスの不透明性」
2. 課題:微細な3D構造の造形限界と評価手法の欠如
3. 解決:BMFのPµSL技術による高精度デバイスの実現
4. データ検証:粒子形成プロセスの「その場観察」に成功
5. まとめ:合理的設計による次世代DDS開発への貢献
フランクフルト大学の研究チームは、BMFの超高解像度3Dプリンター「microArch S240」を活用し、マイクロ流体デバイス内部での流体挙動と脂質ナノ粒子(LNP)形成をリアルタイムで観察する革新的な手法を開発しました。
本研究成果は、「In situ imaging of fluid dynamics and nanocarrier nucleation inside microfluidic mixing devices」というタイトルで、学術誌 『Lab on a Chip』 に掲載されました。
1. 背景:ナノ医薬品の産業化を阻む「製造プロセスの不透明性」
mRNAワクチンなどに代表されるナノ粒子ベースの ドラッグデリバリーシステム(DDS) において、マイクロ流体デバイスを用いた「ナノ沈殿法」は、高品質な粒子を安定生産するための鍵となります。
しかし、デバイス内部で「いつ、どこで、どのように」粒子が形成されるのかというナノ粒子形成メカニズムの詳細については、これまで十分な解明が進んでいませんでした。
2. 課題:微細な3D構造の造形限界と評価手法の欠如
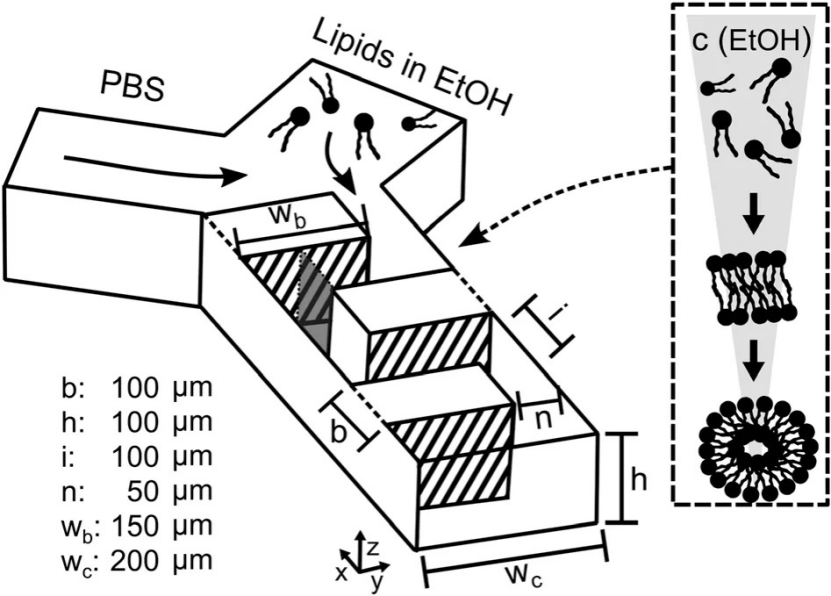
ナノ粒子のサイズを精密に制御するためには、流路内に複雑な「バッフル(邪魔板)」を設けて混合効率を高める必要があります。
しかし、従来の加工技術では、マイクロスケールの精密なマイクロ流体ミキサー構造を柔軟かつ迅速に試作することに限界がありました。
また、従来の評価手法(蛍光染料の追跡等)は間接的な情報に留まっており、粒子形成プロセスを直接監視できる新たな分析プラットフォームが求められていました。
3. 解決:BMFのPµSL技術による高精度デバイスの実現
精密なプロトタイピング
超高解像度3Dプリンター「microArch S240」を用いることで、数百ミクロン幅の流路内に、設計通り20個の微細な長方形バッフルを配置した金型(モールド)を極めて高い再現性で製作しました。
マルチモーダル分析の統合
製作されたデバイスをベースに、共焦点ラマン顕微鏡、共焦点蛍光顕微鏡、およびFRET(フェルスター共鳴エネルギー移動)顕微鏡を組み合わせ、流体とナノ粒子の挙動を同時に捉える環境を構築しました。
4. データ検証:粒子形成プロセスの「その場観察」に成功
BMFの技術によって実現した マイクロ流体デバイス により、以下の検証結果が得られました。
優れた造形精度
SEM(走査電子顕微鏡)観察により、バッフル構造の寸法誤差が5%以下という極めて高い精度で造形されていることが確認されました。
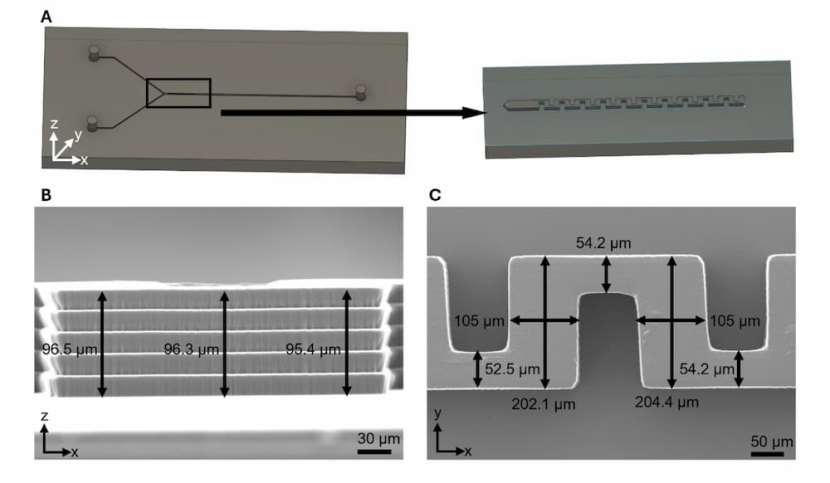
図S1 SEMによる3Dプリント構造の造形精度評価
A:ソフトリソグラフィー用モールドのCAD設計(左)と、SEM観察用に作製された小型モールド(右), B:小型モールドの x–z 断面構造, C:小型モールドの x–y 平面構造
粒子サイズの制御
全流量(TFR)の調整により、脂質ナノ粒子(LNP) のサイズを 116nmから45nm まで意図した通りに制御できることを実証しました。
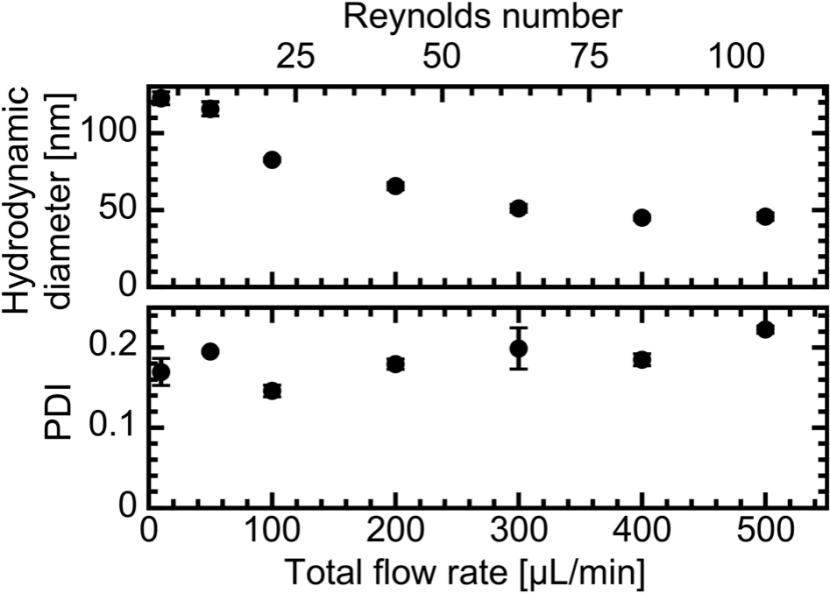
図2 総流量(TFR)とナノ粒子サイズの関係
核生成の可視化
FRET顕微鏡を用いることで、溶媒が混合される過程で脂質が自己組織化し、ナノ粒子が形成(核生成)される瞬間をデバイス内部で空間的に特定することに成功しました。
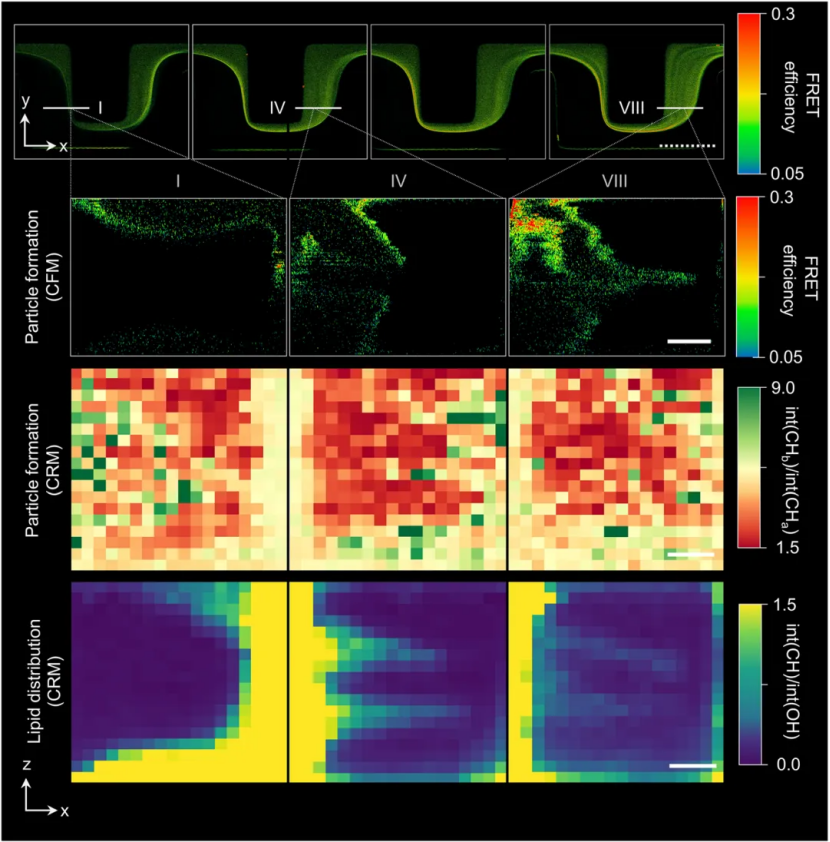
図3 FRET顕微鏡およびラマン顕微鏡による脂質ナノ粒子形成プロセスの可視化
5. まとめ:合理的設計による次世代DDS開発への貢献
本研究は、BMFの超高精度3Dプリンティング技術が、複雑なマイクロ流体デバイスの迅速な試作だけでなく、ナノ医薬品の製造プロセス解明において不可欠なツールであることを示しました。
この成果により、経験則に頼らない「合理的なデバイス設計」が可能となり、創薬研究から大規模な商用生産に向けたスナノ医薬品開発 の加速が期待されます。
装置仕様や研究用途でのご相談は、どうぞお気軽にお問い合わせください。
【引用文献】